Лаборатория геологии техногенных процессов
Болотина И.Н., Воронкевич С.Д., Максимович Н.Г. О возможности техногенных биогеохимических явлений при силикатизации гипсоносных пород // Вестн. Моск. ун-та.-1986.-Сер.4. Геология. N4.-С.49-53.
О ВОЗМОЖНОСТИ ТЕХНОГЕННЫХ БИОГЕОХИМИЧЕСКИХ ЯВЛЕНИЙ ПРИ СИЛИКАТИЗАЦИИ ГИПСОНОСНЫХ ПОРОД
И. Н. Болотина, С. Д. Воронкевич, Н. Г. Максимович
Широкое применение химических инъекционных растворов для закрепления и уплотнения пород при строительстве инженерных сооружений обусловливает необходимость изучения процессов, происходящих и образующихся при этом техногенно-геохимических системах [3]. В продолжение работ, проведенных но изучению постинъекционных процессов при доуплотнении противофильтрационной завесы Камской ГЭС [7], были выполнены микробиологические исследования.
О присутствии значительных количеств микроорганизмов в грунтах свидетельствуют данные ряда авторов [l, 2, 9], с подземными водами они проникают на глубину до нескольких километров [4]. Микроорганизмы способны осуществлять многие процессы, которые не могут происходить химическим путем, оказывая тем самым влияние на основные физико-химические параметры среды. Наиболее заметно деятельность микроорганизмов проявляется в местах с повышенным содержанием органических веществ, микробиологическое разложение которых ведет к обильному выделению газов, накоплению продуктов неполного разложения органики и др. О протекании подобных процессов при строительстве инженерных сооружений свидетельствуют, в частности, данные А. M. Кузнецова [6] об обильном выделении газов (СН4, H2S, CO2, H2 и др.) после сооружения плотины Камской ГЭС. Источниками органического вещества для микробиологического образования газов в основании плотины являлись: органическое вещество пород; богатые органикой воды, фильтрующиеся из водохранилища; гидроизоляция подземных сооружений, представляющая собой мешковину, пропитанную битумом, и др. Начатое в 1974 г. доуплотнение цементационной завесы щавелевоалюмосиликатным (ЩАС) гелем, имеющим в своем составе производные органической кислоты, создало дополнительный источник питания для микроорганизмов. В связи с этим проведены исследования для оценки принципиальной возможности проявления биогеохимических процессов в условиях формирующихся техногенно-геохимических систем.
Объекты и методы исследования. Объектами исследования являлись природные воды и ЩАС гель, приготовленный в лабораторных условиях. Пробы воды были отобраны из трех пьезометрических скважин в основании Камской ГЭС и имели различный химический состав и минерализацию: из скв. 2256 — сульфатно-натриевые 2,5 г/л; из скв. 248 — сульфатно-натриевые 5,5 г/л; из скв. 118 — хлоридно-натриевые 33,6 г/л. Температура вод 7—8 °С, значения водородного показателя после создания завесы 7,2—8,0. Из проб производилось выделение микроорганизмов методом предельных разведений на среду Виноградского для сульфатредуцирующих бактерий в модификации Кочкиной и методом высева из разведений на агаризованный грунт [8].
Среда Виноградского имеет следующий состав (г/л): КН2РO4 — 0,05; MgS04 — 2,5; NaCl — 2,5; FeSO4 — 0,05; MnSO4 — 0,05; бумага фильтровальная, измельченная на тканеизмельчителе — 2,5; рН 7,2. Агаризованный грунт готовили из загипсованного лёссового грунта, отношение грунт : водопроводная вода — 1:5, агар-агар — 2%.
Приготовление образцов ЩАС геля для лабораторных исследований проводили при соотношении силиката натрия и отвердителя, соответствующих применяемым при инъекции в основании Камской ГЭС (100:46). Раствор готовили из двух составляющих: силиката натрия плотностью 1,19 г/см3 и отвердителя, представляющего собой водный раствор сернокислого алюминия (50 г/л) и щавелевой кислоты (50 г/л). Приготовленный раствор, имеющий рН 11,1—11,6, заливали в чашки. Петри и через 1,5 ч после образования геля отмывали дистиллированной водой до значений водородного показателя промывочного раствора, близких к нейтральным. Отмывка производилась для придания интермицеллярной жидкости геля значений рН, реально существующих в массиве. Были поставлены следующие варианты опытов.
Вариант 1. На поверхность геля в чашке Петри насыпали тонкий слой порошка гипса, отобранного из скважин в основании Камской ГЭС. Затем в чашку добавляли воду из скв. 118, содержащую микроорганизмы. Вода имела следующий химический состав: Са2+ — 2; Mg2+ — 0,8; Na+ — 9,8; Cl- — 13,4; SO42- — 8,4; НСО3 — 0,01; СО32- — 0,002 г/л.
Вариант 2. Кроме порошка гипса поверхность геля покрывали, слоем фильтровальной бумаги, являющейся источником органического питания для микроорганизмов, и заливали суспензией культуры сульфатредуцирующих бактерий, выделенных из подземных вод Камской ГЭС.
Вариант 3. Ингредиенты те же, что в варианте 2, но в качестве микробной культуры использовали активный штамм сульфатредуцирующих бактерий, выделенный из почвы.
Внесение гипса во все варианты опытов обусловлено тем, что в закрепляемых породах основания плотины Камской ГЭС содержится значительное количество гипса, который может служить акцептором электронов при получении энергии сульфатредуцирующими бактериями. Чашки Петри с образцами выдерживали в анаэростате в течение 10 месяцев. Затем производили исследование геля на сканирующем электронном микроскопе КВИКСКАН-107 и на рентгеновском дифрактометре ДРОН-0,5. Электронно-микроскопическое изучение проводили после замораживания образцов геля в жидком азоте и сублимационной сушки в вакууме.
Результаты исследований и их обсуждение. Применение в качестве питательных сред агаризованного грунта и среды Виноградского показало, что в водах основания Камской ГЭС содержится значительное количество микроорганизмов, в том числе сульфатредукторы, бактерии, окисляющие Fe и Мn, неспоровые пигментированные и бесцветные бактерии, количество которых достигает 103 клеток/мл. Часть из этих микроорганизмов способна развиваться, используя компоненты ЩАС геля.
В условиях, наиболее приближенных к природным. (вариант 1). бактерии, содержащиеся в воде из скв. 118, образовали колонии как на поверхности геля, так и внутри него, вплоть до дна чашки. При этом примерно одна треть объема геля, имеющего белый цвет, приобрела темную окраску и сильный запах Н2S. Темная окраска обусловлена отложением сульфидов, образующихся в результате взаимодействия сероводорода, с металлами, содержащимися в среде, и в первую очередь с железом. Гладкая поверхность геля стала шероховатой. Микробиологический посев из почерневших участков геля и их электронно-микроскопическое изучение свидетельствовали о микробном происхождении отложений черного цвета и о принадлежности этих организмов к группе сульфатредуцирующнх бактерий. Полученные результаты и отчетливый запах сероводорода подземных вод изучаемых участков Камской ГЭС, а также имеющийся в них черный осадок сульфидов явились основанием для особого внимания при изучении этой группы микроорганизмов.
С деятельностью сульфатредуцирующих бактерий уже с конца прошлого века связывают процессы восстановления сульфатов, образование сероводорода и серы в биосфере. Восстановление сульфатов способны осуществлять многие факультативные анаэробы. Способность использовать сульфаты в качестве конечного акцептора электронов с образованием больших количеств сероводорода присуща лишь высоко-специализированной группе микроорганизмов — облигатно анаэробным сульфатредукторам, к которым относятся гетеротрофные бактерии родов Desulfovibrio и Desulfotomaculum, а также некоторые другие, обнаруженные в последнее время организмы [5]. В анаэробных условиях или при ограниченном доступе воздуха в процессе жизнедеятельности сульфатредуцирующих бактерий органические вещества (углеводы, органические кислоты) подвергаются дегидрогенизации, водород переносится на сульфаты, сульфиты или тиосульфаты, которые восстанавливаются в сероводород. При этом образуются уксусная кислота и сероводород:
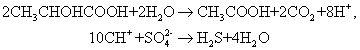 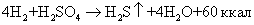 . Образующийся сероводород активно взаимодействует как с твердой фазой грунта, так и с имеющимися в жидкой фазе катионами. Он осаждается и выделяется в виде нерастворимых сульфидов металлов, например FeS, что может существенно повлиять на свойства грунта.
Чтобы ускорить происходящие в природе процессы микробиологического восстановления сульфатов с образованием сероводорода, нами были созданы условия, способствующие активной жизнедеятельности сульфатредуцирующих бактерий. С этой целью были внесены дополнительные источники органического питания (фильтровальная бумага), минерального питания (минеральные соли) и энергии (гипс). В этих условиях развитие сульфатредукторов и образование сульфидов происходили наиболее интенсивно (варианты 2 и 3), особенно при использовании коллекционного штамма. В последнем случае (вариант 3) гель потерял упругость, приобрел черную окраску и сильный запах сероводорода; покрывающий гель лист фильтровальной бумаги был сильно изъеден, его поверхность уменьшилась на 1/3. Рентгенометрическое изучение почерневших участков геля, подвергшихся наибольшему изменению, показало отсутствие в них кристаллической фазы.
Электронно-микроскопическое изучение образцов вариантов 2 и 3 показало значительную неоднородность геля в местах развития микроорганизмов: относительно неизмененные участки (рис. 1, а) чередовались с участками, содержащими дополнительный биогенный компонент (рис. 1, б-г), количество которого было больше в варианте 3. В основном это нитевидные структуры, покрытые аморфными отложениями (рис. 1, г). Более молодые клетки не имеют толстого чехла (рис. 2). Изучение образцов геля варианта 1, условия в котором были максимально приближены к природным, не выявило заметных отличий в структуре геля по сравнению с исходными.
Таким образом, формирование и эволюция специфической техногенно-геохимической обстановки в результате инъекции гелеобразующих растворов, содержащих органическое соединение, в определенных условиях (в данном случае в присутствии гипса) могут оказаться благоприятными для возникновения и развития соответствующих биогеохими-ческих процессов. Для оценки инженерно-геологического значения обнаруженного авторами явления, и в частности его влияния на характер и интенсивность постинъекционных процессов, определяющих наиболее существенные физико-механичсские и фильтранные свойства системы, требуются дополнительные лабораторные исследования и натурные наблюдения. . Образующийся сероводород активно взаимодействует как с твердой фазой грунта, так и с имеющимися в жидкой фазе катионами. Он осаждается и выделяется в виде нерастворимых сульфидов металлов, например FeS, что может существенно повлиять на свойства грунта.
Чтобы ускорить происходящие в природе процессы микробиологического восстановления сульфатов с образованием сероводорода, нами были созданы условия, способствующие активной жизнедеятельности сульфатредуцирующих бактерий. С этой целью были внесены дополнительные источники органического питания (фильтровальная бумага), минерального питания (минеральные соли) и энергии (гипс). В этих условиях развитие сульфатредукторов и образование сульфидов происходили наиболее интенсивно (варианты 2 и 3), особенно при использовании коллекционного штамма. В последнем случае (вариант 3) гель потерял упругость, приобрел черную окраску и сильный запах сероводорода; покрывающий гель лист фильтровальной бумаги был сильно изъеден, его поверхность уменьшилась на 1/3. Рентгенометрическое изучение почерневших участков геля, подвергшихся наибольшему изменению, показало отсутствие в них кристаллической фазы.
Электронно-микроскопическое изучение образцов вариантов 2 и 3 показало значительную неоднородность геля в местах развития микроорганизмов: относительно неизмененные участки (рис. 1, а) чередовались с участками, содержащими дополнительный биогенный компонент (рис. 1, б-г), количество которого было больше в варианте 3. В основном это нитевидные структуры, покрытые аморфными отложениями (рис. 1, г). Более молодые клетки не имеют толстого чехла (рис. 2). Изучение образцов геля варианта 1, условия в котором были максимально приближены к природным, не выявило заметных отличий в структуре геля по сравнению с исходными.
Таким образом, формирование и эволюция специфической техногенно-геохимической обстановки в результате инъекции гелеобразующих растворов, содержащих органическое соединение, в определенных условиях (в данном случае в присутствии гипса) могут оказаться благоприятными для возникновения и развития соответствующих биогеохими-ческих процессов. Для оценки инженерно-геологического значения обнаруженного авторами явления, и в частности его влияния на характер и интенсивность постинъекционных процессов, определяющих наиболее существенные физико-механичсские и фильтранные свойства системы, требуются дополнительные лабораторные исследования и натурные наблюдения.
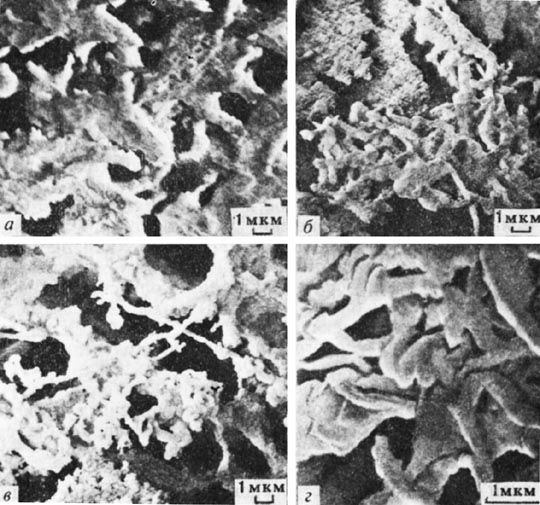
Рис. 1. Щавелевоалюмосиликатный гель, подвергнутый микробиологическому: а — неизменный участок; б-г — биогенный компонент в структуре геля
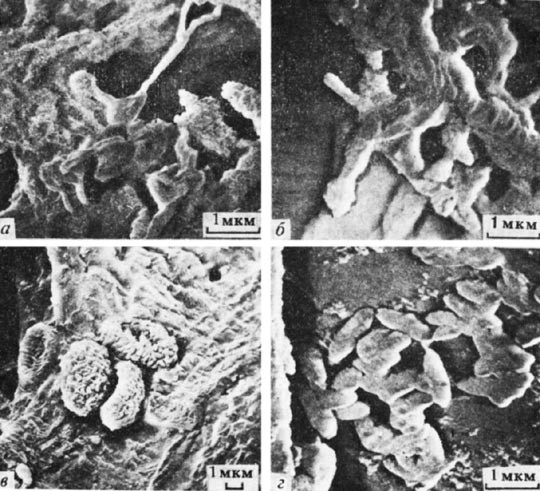
Рис. 2. Клетки микроорганимов в системе ЩАС—гипс—вода
СПИСОК ЛИТЕРАТУРЫ

|
|
|

